√100以上 周期表 原子番号 質量数 111988-周期表 原子番号 質量数
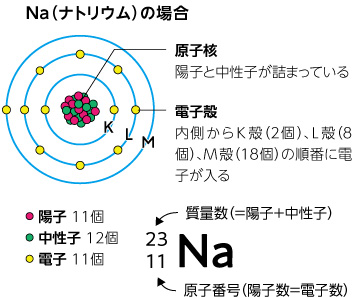
質量数=陽子の数中性子の数 原子番号=陽子の数(=電子の数) 〈例〉 質量数 原子番号 c 12 6 中性子の数は質量数−原子番号で求められる。 同位体(アイソトープ) 原子番号が同じで質量数の異なる原子どうし。同位体どう 原子番号≠原子量 どちらも「原子」がつくのでよく間違える。 原子番号は陽子数。 原子番号順に並べたのが周期表。 周期表の横の行は周期、縦の列は族。 同じ族の元素で、 価電子数が等しく、 化学的性質が似ている仲間が同族元素。原子番号:陽子の数。 質量数:陽子の数と中性子の数の和。 原子番号(陽子の数)は元素ごとに決まっている。 また,陽子の質量と中性子の質量はほぼ等しく, 電子の質量は陽子や中性子の質量に比べて非常に 小さい。

元素周期表 見やすい表で覚え方と元素を解説 ゴロ合わせも 高校生向け受験応援メディア 受験のミカタ
周期表 原子番号 質量数
周期表 原子番号 質量数-周期表の左2列は s 軌道, 右2行が p 軌道, 残りが d 軌道です。例えば, 周期4の第7族は, 3d 軌道が案内中の座席です。このとき, 1s軌道, 2s軌道, 2p軌道, 3s軌道, 3p軌道, 4s軌道 は満席になっています。各軌道の席数は, 周期番号 (主量子数) に関わらず, s 軌道が2席, p質量数と原子番号 元素記号の左上には、質量数を書き、左下には原子番号を書く。原子番号はその元素の持つ陽子数に等しい。質量数は、陽子と中性子の数の和に等しい。 原子(Atom)の構造と周期表 原子
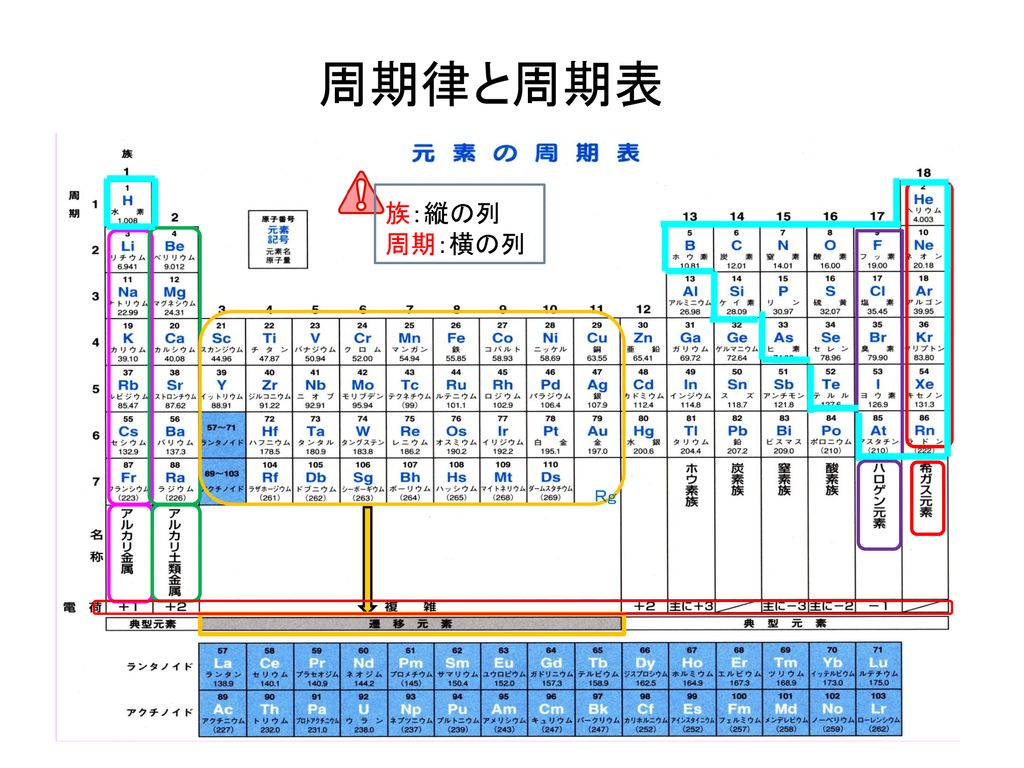



教養の化学 第4週 2013年10月14日 担当 杉本昭子 Ppt Download
元素記号と周期表 原子の構造 – 原子核(陽子、中性子)、電子 – 原子番号 – 質量数 – 同位体 生体の主な構成元素(%)p2 地殻の元素の存在比(%) 地球と宇宙の元素の存在比(%) 一家に1枚周期表 元素の周期表 1族2族3族4族5族6族7族8族9族 10原子 原子番号 質量数 陽子の数 中性子の数 電子の数 h &o 8 ア イ ウ エ オ カ 元素の一覧 Wikipedia 本項では、標準的な周期表に記述される元素を元素の一覧(げんそのいちらん)として概説する。陽子の数(原子番号)で化学的性質が決まります は、その元素の代表的な放射性同位体の質量数である(iupac) 文部科学省 「一家に一枚周期表第6版」 原子は原子核とその周りを回る電子から構成されています。 とに質量数(陽子と中性子の合計数
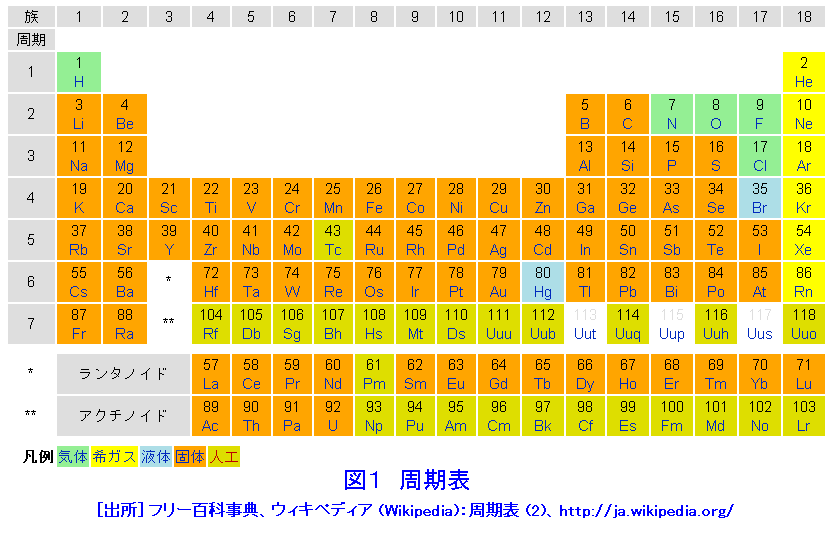
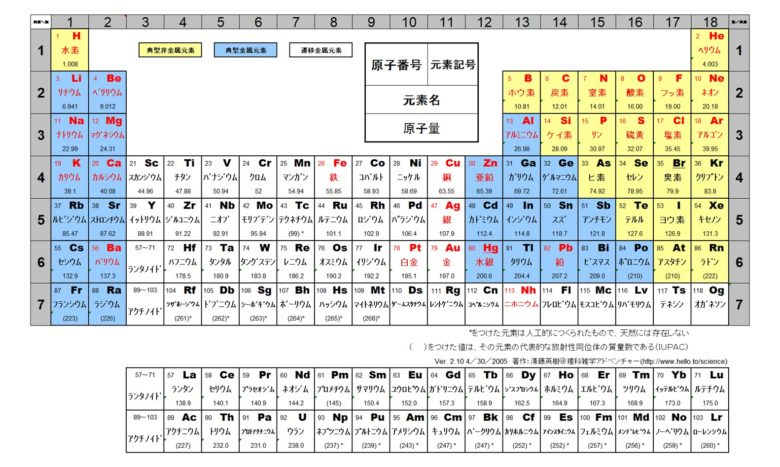
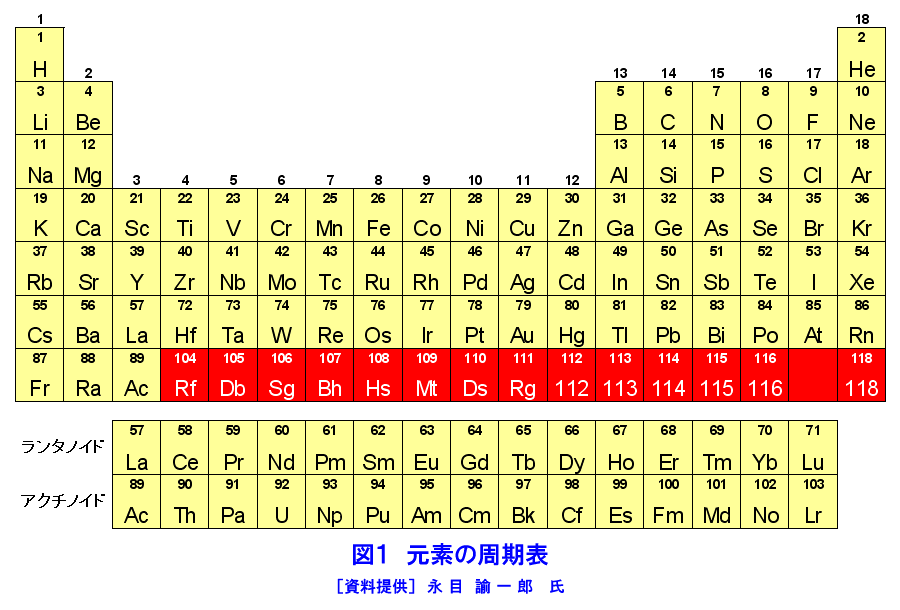
原子核の性質によって 様々な壊変の様式 があります. 代表的な例をいくつか紹介します. α壊変 ある原子Xの原子核から 4 He原子が飛び出す壊変をα壊変といいます。 この 4 Heはα線と呼ばれます。 Xは原子番号が2,質量数が4小さい原子Yへと変換します。 図1 元素周期表(21年6月現在) 原子番号が104を超える元素は超アクチノイド元素または超重元素と呼ばれ、合成には大型加速器を用いた核反応を必要とする。 本研究で対象とした105番元素ドブニウム(Db)は、41番元素ニオブ(Nb)および73番元素タンタル(Ta)とともに周期表第5族に属する超Ra ラジウム (226) –103 7 Ac アクチニウム (227) 90 Th トリウム 234 91 Pa プロトアクチニウム 92 U ウラン 93 Np ネプツニウム (237) 94 Pu プルトニウム (244)
( 2 ) 1編2章_原子の構造と元素の周期表_生徒用 B. 位体 原子番号は じだが,原子核中の中性子の数が異なるため質量数の異なる原子ど うしを,互いに( 位体(アイソトープ) )であるという。 例)水素の 位体には質量数1の1h と,2の2h,3の3h が存在する。 位体は( 質量 )は異なるが,その化学的な( 性質 )はほぼ じ。原子番号 元素名 元素記号 原子量 1 水素 H (7) 2 ヘリウム He (2) 3 リチウム Li 4 ベリリウム Be (3) 5 ホウ素 B (7) 6 炭素 C 1107 (8) 7 窒素 N (2) 8 酸素 O (3) 9 フッ素 F (5) 10 ネオン Ne 1797 (6) 11 ナトリウム Na 22原子量から原子番号を引く 原子量から原子番号(=陽子数)を引いた数が中性子数となります。 5 X 出典文献 例:ホウ素の中性子数の求め方は、11 (原子量) – 5 (原子番号) = 6になります。




30 01 5 Lihat Cara Penyelesaian Di Qanda



No 264 ダレナン博士の研究所
同位体どういたい 原子番号が同じで質量数が異なる核種。 周期表で同じ位置に入る 元素 という意味で,同位元素あるいはアイソトープともいう。 たとえば水素には,大部分を占める 1 Hのほか重水素 2 H(ジューテリウムD), 3 H(トリチウムT)がある。 自然界の元素の多くはいくつかの同位体からなり(Al,F,Naなどは例外),それらの異なる同位体の存在塩 周期表を同一周期内で左から右に進むと,原子中の電子の数が増加する。 於 原子の第一イオン化エネルギーは,原子番号の増加とともに,周期的に変化する。 汚 陽子の数が等しい原子は,質量数が異なっても,周期表上で同じ位置を占める。 原子 原子殻 原子の構造まとめ文 イオン 原子の陽性・陰性 原子 原子:ドルトンが提唱した物質を構成する最小の粒 原子核:原子の中心にあり、正()の電気を帯びた陽子と電気を帯びていない中性子からできている。陽子の数で原子の種類が決まっている。
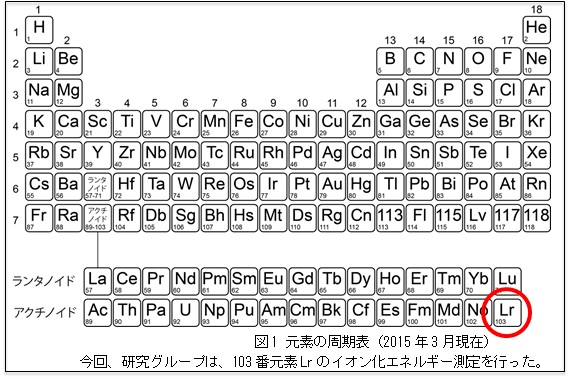



103番元素が解く 周期表のパズル ローレンシウム Lr のイオン化エネルギー測定に成功 日本原子力研究開発機構 プレス発表




サイエンスの祭り 国際周期表年が終わっちゃいますよー どこでもサイエンス 169 Tech
©12日本化学会 原子量専門委員会 原 子 量 表 (12) (元素の原子量は,質量数12の炭素( 12c)を12とし,これに対する相対値とする。但し,この 12cは核および電子が基底状態にある結合してい ない中性原子を示す。 元素の原子量または原子量 ほとんどの周期表には、 各元素タイルの 原子量 ( 原子量 とも呼ばれます)の値が含まれています 。 元素の単一の原子の場合、これは整数になり、原子の陽子、中性子、および電子の数が加算されます。 ただし、周期表に記載されている値 は、特定の元素の すべての 同位体 の 質量の平均です 。 電子の数は原子に大きな質量を与え周期表の重要性 科学 21 周期表は、化学の歴史の中で最も重要なツールの1つです。 原子番号、原子質量、元素間の関係など、既知のすべての化学元素の原子特性を簡潔な形式で記述します。 同様の化学的性質を持つ元素は、周期表の列に配置されます




ダウンロードまたは印刷する無料のpdf化学ワークシート
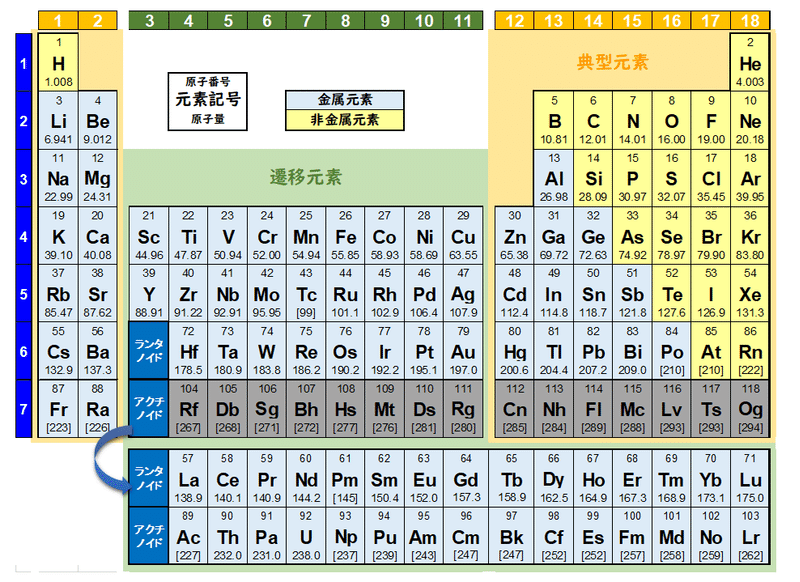



1 6 元素の周期律と周期表 おのれー Note
原子番号と質量数の関係! Drあゆみの物理教室 原子の構造! 原子番号と質量数の関係! 世の中のあらゆるものは、『 原子 (げんし) 』というとっても小さい粒々からできています。 私たち人間も、毎日食べているご飯も、机も、パソコンやスマホも周期表では元素は何の順番にならべてあるか。 そんな理由から原子番号順になっています。 よくみると原子量の大きさが逆なところがありますが、同位体の影響です。 質量数が同位体の中性子の数が違うために物質はひとつの質量にはなりません。1 原子核の崩壊 周期表を眺めて原子番号の大きい元素の質量数に注目してみよう.たとえ ばラジウムの質量数は226,のウランの質量数は238,プルトニウムの質量数 は239といった値である.このように,陽子と中性子をあわせて8個以上
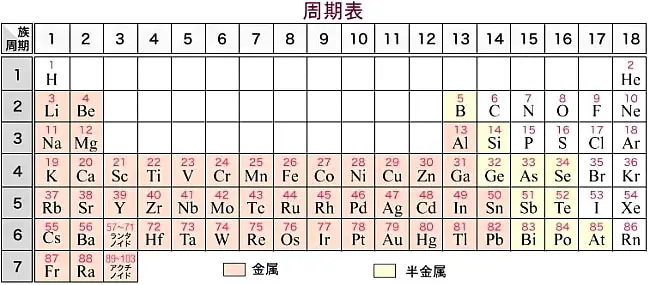



万物は元素で出来ている p1




元素周期表 Monozukuri Hitozukuri 日本のものづくり
子番号すなわち原子核の陽子の数の順に並ぶ周期表のコン セプトが固まることになる。さらに,周期表の構成に変革 を迫ったのは,希土類の位置づけと同位体の発見である が,ここでは触れない。 いずれにしても,周期表は化学の中で最大の発明であり同じ元素の原子は全て核に同数の陽子を持ちます。この数を原子番号(atomic number)と呼び、記号Z で示します。教科書の裏表紙の周期表では、各元素の原子番号は元素記号の上に示されています。例えばナ トリウム原子は11個の陽子を含む核を持ち、原子番号現在の周期表では,原子番号(=陽子の数)の順に並んでいる。 ・原子の質量と原子番号が逆転しているもの 同位体の天然存在率によって異なる 例 Ar(400)と K(391) Co(5)と Ni(587) Te(1276)と I (1269) 50分 第1章のキーワード:元素の周期表,周期,族,典型元素・遷移元素,周期律,
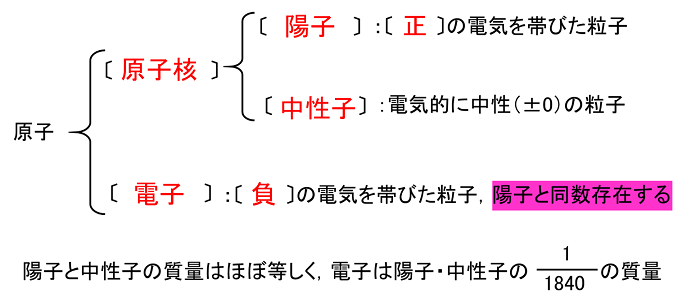



原子とその構造




質量数とは 求め方と原子番号との関係をまとめてみた 化学受験テクニック塾
1 左上から右下に向かって読む 周期表では原子番号の順に元素が並んでいて、左から右、また上から下に行くほど原子番号が大きくなります。 原子番号はその元素の原子内の陽子の数です。 また、各元素の原子の質量は、周期表の左から右に行くほどポイントの解説授業 今回のテーマは、「原子番号と質量数」です。 まずは、原子の表し方から学習していきましょう。 図を見てください。 左には 野球選手 がいますね。 野球選手の背中には、 背番号 があります。 この選手の場合は「1」が与えられていますよね。 それぞれの選手に 別々の番号を与えることで、選手を区別することができる ようになってい 周期表には周 横の並びを上から1周期 (水素とヘリウム)、2周期 (リチウムからネオンまで)、3周期、4周期、5周期と並んでいます。 3周期までは、横の並びで電子が最外殻に一つずつ順番に充填されていくのが判ります。 周期表は、元素が原子番号 (陽子数)が増える従い、電子がその電子軌道にどのように充填されていくのかを知らないと理解していくのは難しい



1




周期表暗記のコツは 現役東大生が高校化学で必須の元素の覚え方を語呂合わせで紹介 学びtimes
Start studying 質量数と周期表 Learn vocabulary, terms, and more with flashcards, games, and other study toolsHe原子 電子 陽子 中性子 電荷 1 ** 1 0 質量/kg 9109×1031 1673×1027 ×1027 1 17 19 広がり/m 0529×1010* 12×1015 12×1015 1 1 *ボーア半径 ** 1602×1019 C 原子を化学辞典 第2版 テクネチウムの用語解説 Tc.原子番号43の元素.人工放射性元素.電子配置Kr4d55s2の周期表7族第5周期遷移元素.テクネチウムの同位体は現在,質量数85~118まで知られている.DI Mendeleev(メンデレーエフ)がエカマンガンとして予言していた元素.1925年にW




定期テスト等では 原子番号は提示されないけど 質量数は提示されますよね Clear



モルについて
周期表で確認すると、 ・原子番号2(電子が2個) → He ・原子番号10(電子が10個) → Ne ・原子番号18(電子が18個) → Ar これらの原子は、 周期表の一番右の列 に対応しています。 つまり―― 周期表の一番右の列が、た,a の質量数は原子番号の2 倍であり,b の質量数はa の質量数よりも1 だけ大きい。 この元素x は何かを考え,元素記号で答えよ。(2点) 問4 y は質量数33,中性子数17 の原子であり,z はm 殻に価電子1 個をもつ原子である。周期表の配列は、原子の中心に位置する核が保持する陽子の個数に基づいて付けられる原子番号順に並べられる。 陽子 が1個である 水素 から始まり、1マス進むごとに 陽子 が1つ多い 元素記号 を示しなが
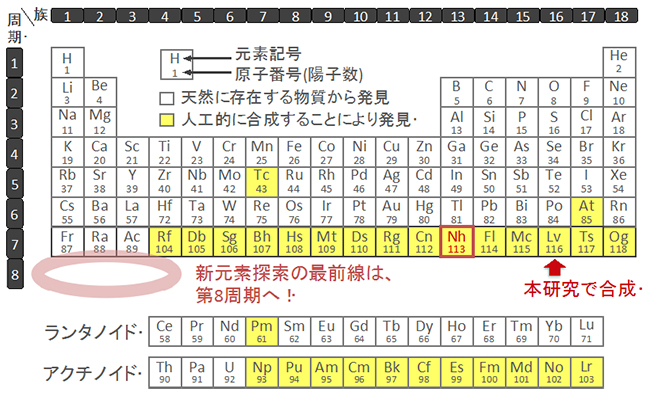



116番元素リバモリウム合成の検証に成功 理化学研究所
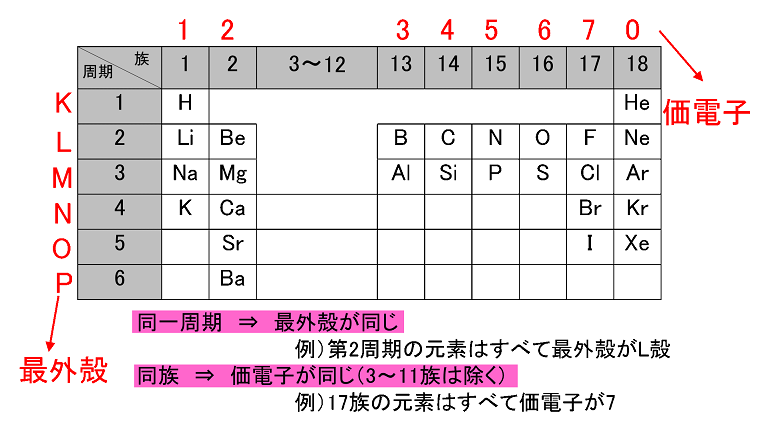



原子とその構造




元素 ラジエーション大学



Q Tbn And9gctxss1qf Ypr6mhpbzjaa Qm17kmboopvpaxrtsilso Teqcwxf Usqp Cau
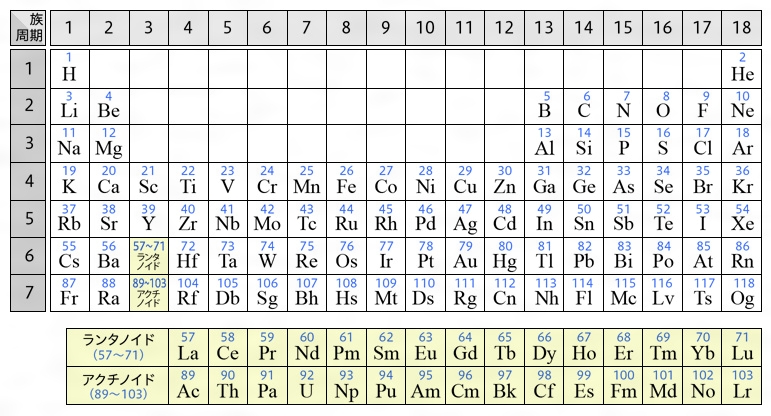



プルトニウムとは コトバンク



原子核と核反応 03 06 01 03 Atomica




化学 原子の構成 周期表 これを読めば時短で簡単に全部わかる Youneed




近代科学 現在注目されている核融合発電 原子の解説 Sakashuの化学




福島第一原発 ヨウ素131 セシウム137とは ナンでもカンでも好奇心 Tomamのブログ




化学基礎 物質の構成16 原子番号と質量数 8分 Youtube




高校化学基礎 原子番号と質量数 映像授業のtry It トライイット




周期表 Wikipedia




Periodex Chromeアプリ 元素記号や日本語の元素名を確認できる周期表アプリ Chrome拡張のいいところ




99以上 元素周期表 壁紙 9107 元素周期表 壁紙



井手禎昭 がん難民をふせぐために わかりやすい 爆発後の日々



Http Www Kyoiku Shuppan Co Jp Textbook Chuu Rika Files Web Syukihyo Pdf




日本が命名した113番元素 ニホニウム 新元素発見までの道のりとこれから Science Portal 科学技術の最新情報サイト サイエンスポータル



化学 周期表 5族 技術情報館 Sekigin 周期表 5族に分類される元素 バナジウム V ニオブ Nb タンタル Ta ドブニウム Db の物性 化学的と特徴を紹介




原子核で元素を読み解く 小林良彦のブログ




高校化学基礎 原子番号と質量数 練習編 映像授業のtry It トライイット
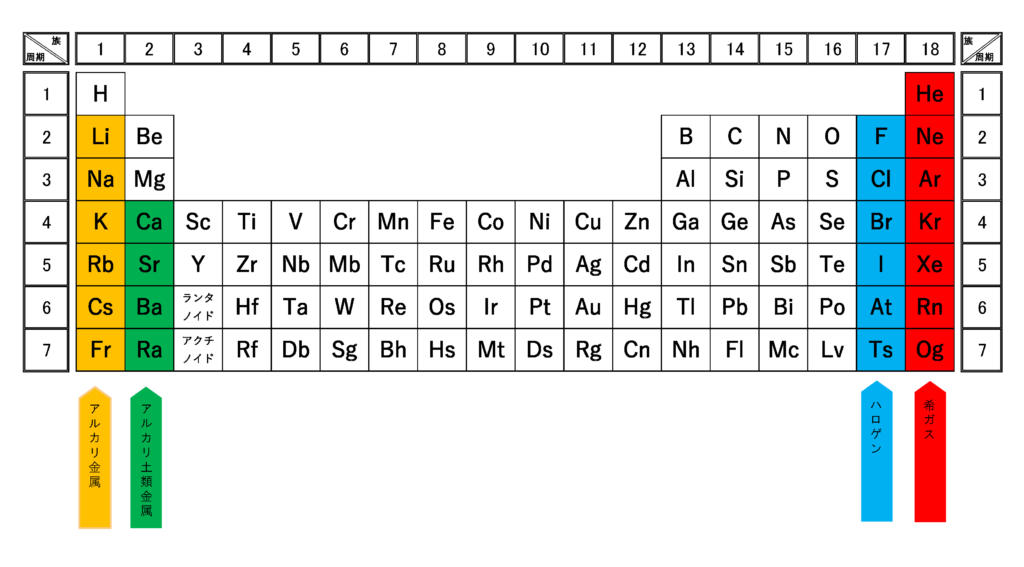



完全版 周期表の語呂合わせの覚え方と族 縦 や周期 横 の見方 サイエンスストック 高校化学をアニメーションで理解する
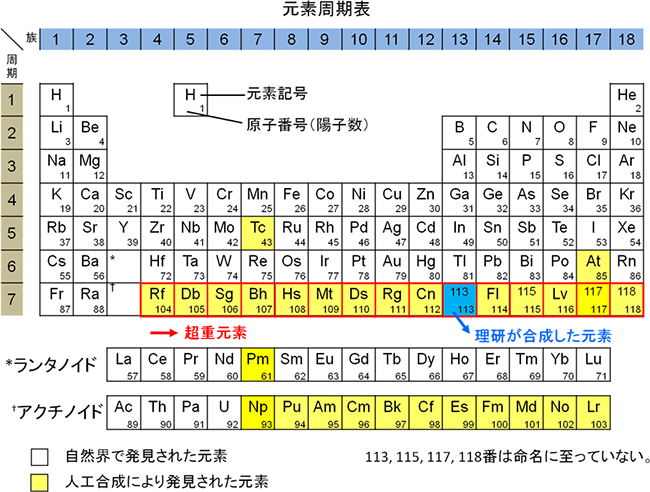



113番元素の命名権獲得 理化学研究所



中2化学 原子と分子 中学理科 ポイントまとめと整理




化学 原子の構成 周期表 これを読めば時短で簡単に全部わかる Youneed



海水中に存在する微量な金属元素の濃度を算出しました その4 海水中で不溶性の元素を選択 水徒然



Q Tbn And9gcqt2b0vsq6wzrzgdbza40ukhx Hky5vf9iiwdmr0ui Usqp Cau




教養の化学 第4週 2013年10月14日 担当 杉本昭子 Ppt Download



超アクチノイド元素の化学的研究 05 01 05 02 Atomica




元素の英語名と読み方一覧表 発音記号とカタカナ読み方付き Yattoke 小 中学生の学習サイト



周期表バンザイ Icemsリサーチスコープ 京都大学アイセムス
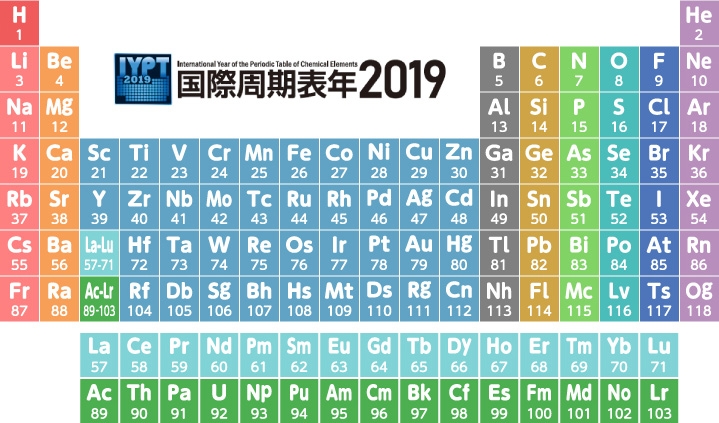



国際周期表年19にちなんで F フッ素 のお話 トピックス ヒカリラボ Photonてらす
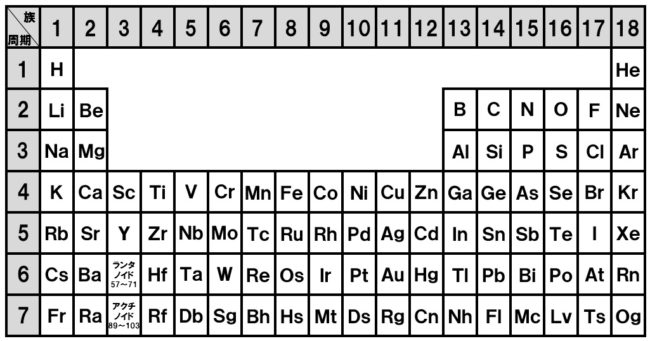



化学基礎 化学基礎で必要な周期表の知識 Tekibo



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Mass Number




Amazon Co Jp Womdee 元素周期表 ビニール周期表 19年版 生徒 先生 化学専門家 ホーム キッチン



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0508 Pdf




53 2 3 1 2 13 14 15 16 Descubre Como Resolverlo En Qanda
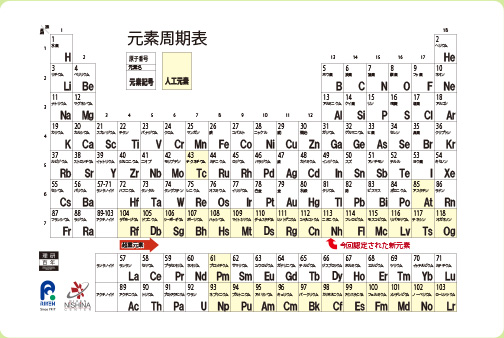



理学研究院 教授 森田 浩介 先生の森 九州大学の個性豊かな先生たちをご紹介 九州大学 Kyushu University




第2回 我々が見つけた 113番元素はここですね ナショナルジオグラフィック日本版サイト
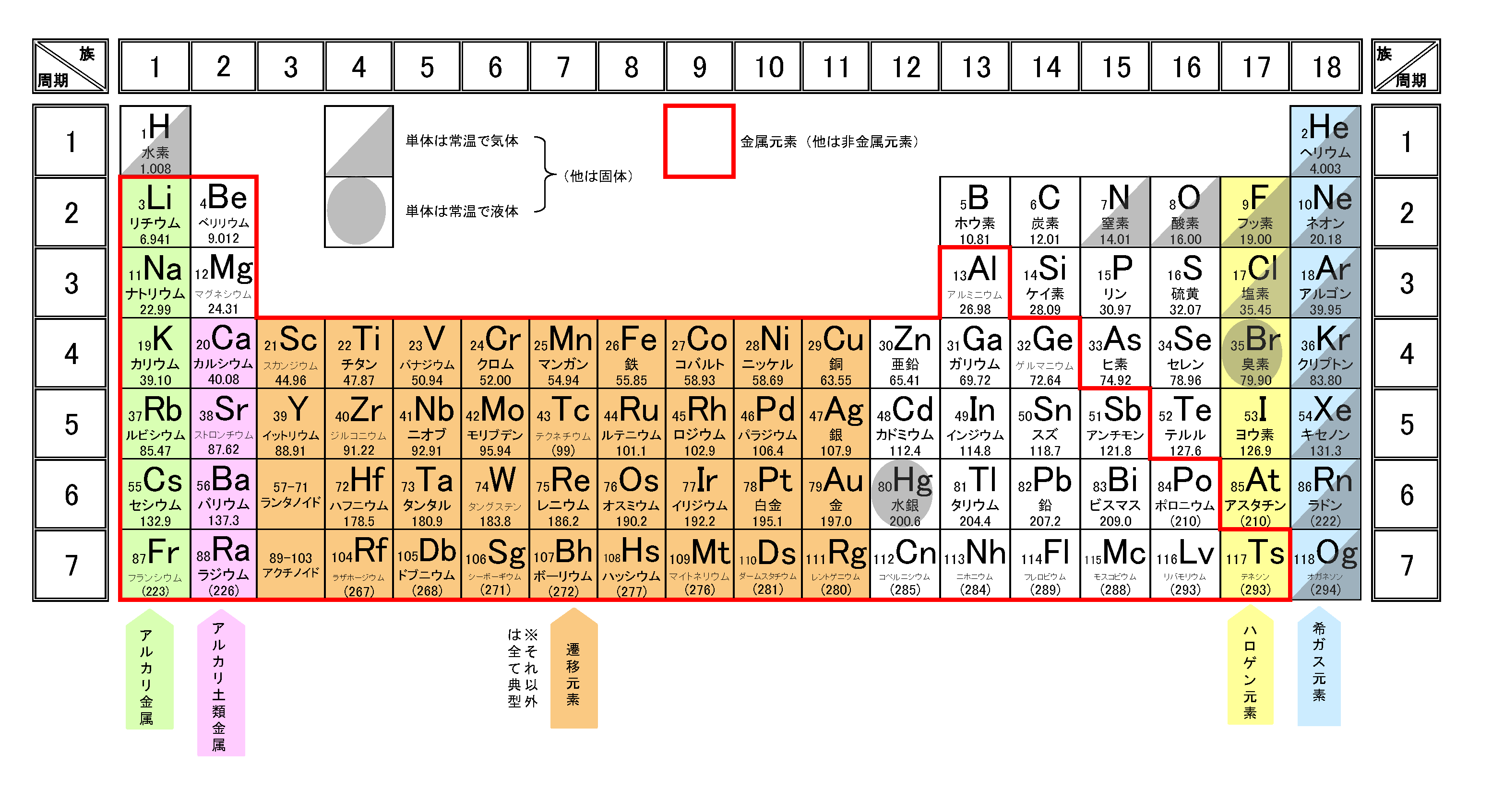



完全版 周期表の語呂合わせの覚え方と族 縦 や周期 横 の見方 サイエンスストック 高校化学をアニメーションで理解する




元素周期表 見やすい表で覚え方と元素を解説 ゴロ合わせも 高校生向け受験応援メディア 受験のミカタ
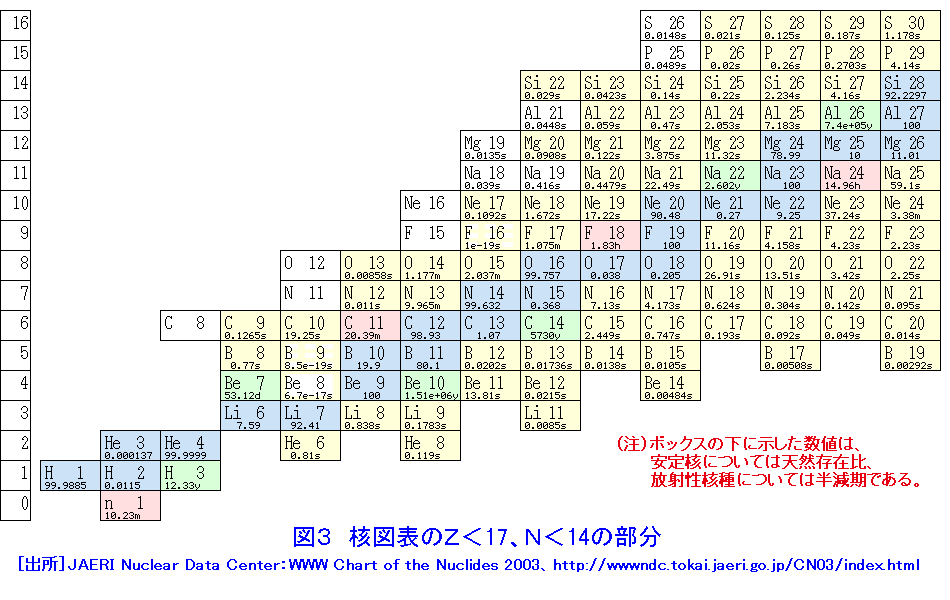



原子核と核反応 03 06 01 03 Atomica




原子番号



Metatronic Metalogue 7 004




第3節 元素の周期表
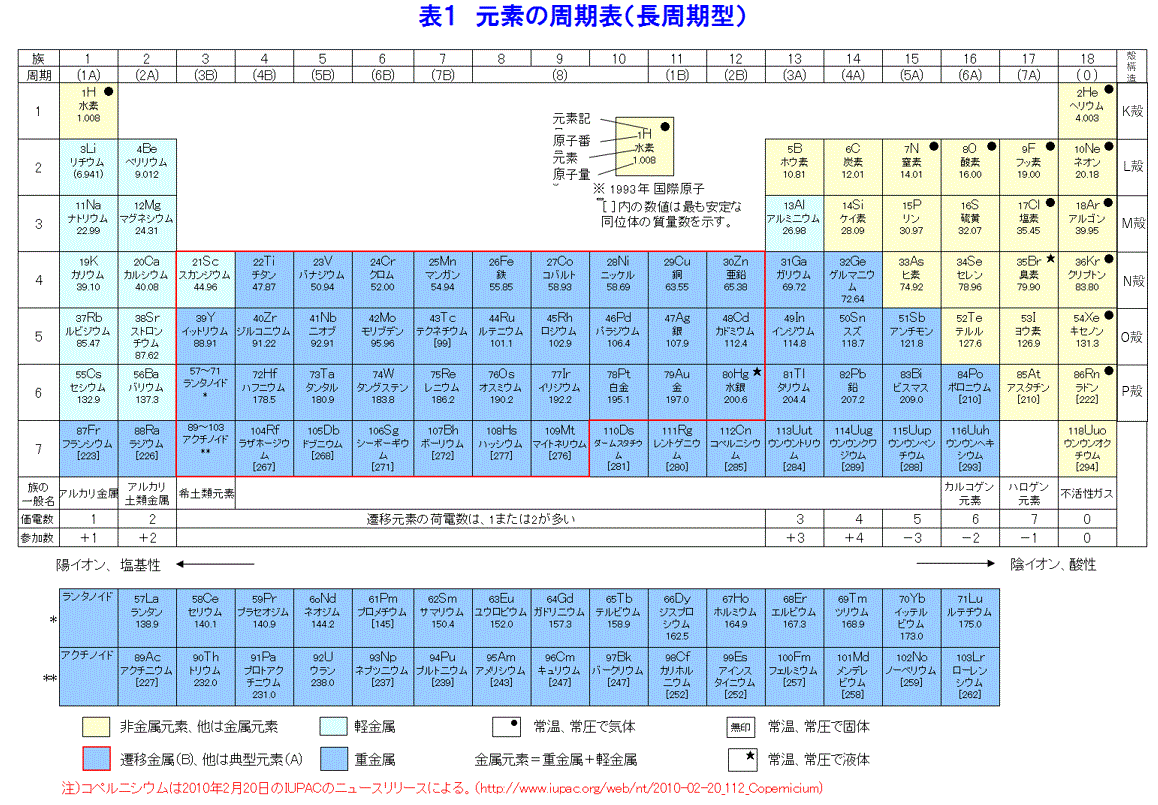



元素の周期表 物性 18 02 01 01 Atomica




元素周期表 見やすい表で覚え方と元素を解説 ゴロ合わせも 高校生向け受験応援メディア 受験のミカタ
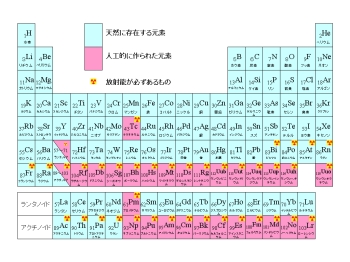



重元素の基礎知識 大阪大学 篠原研究室



周期表と族の特徴を解説してみた 三重の個人契約家庭教師



メディアラボ株式会社 Gperiodic
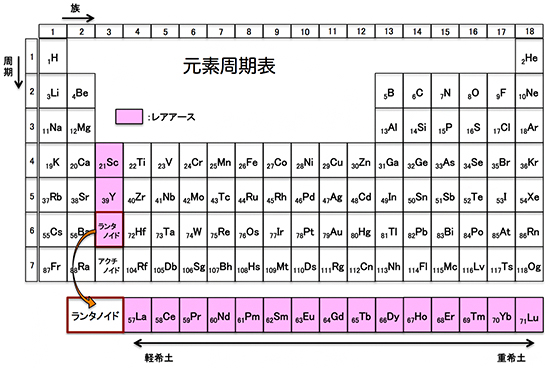



中性子過剰核94種の寿命測定に成功 理化学研究所
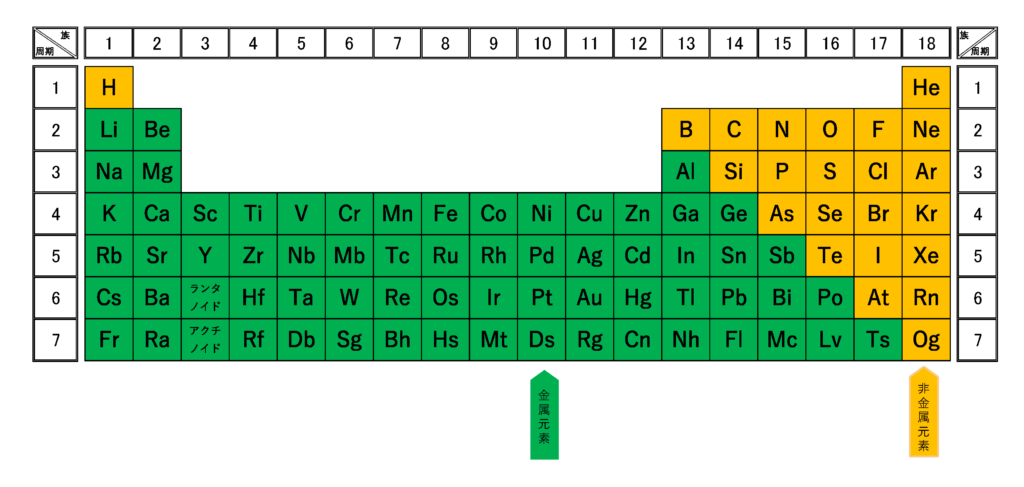



完全版 周期表の語呂合わせの覚え方と族 縦 や周期 横 の見方 サイエンスストック 高校化学をアニメーションで理解する




5分でわかる陽子数 中性子数 数でなにが違う 科学館職員がわかりやすく解説 ページ 3 4 Study Z ドラゴン桜と学ぶwebマガジン




周期表 Wikipedia
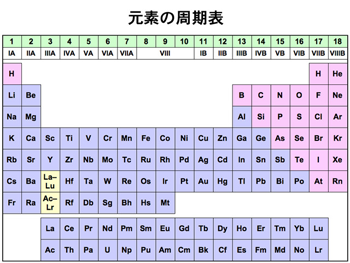



化学入門 理学クエスト ようこそ 探求の世界へ 信州大学 理学部



Www Meigaku Ac Jp Wp Content Uploads 04 78b5d3e712fb0c0a2cedb65a0384 Pdf




周期表の歴史を振り返る 周期表生誕 150 周年特別企画 Chem Station ケムステ




第1章 原子と原子核の中身について考えよう 放射線について考えよう



Q Tbn And9gcqr0ht1ja4n Ldbquu4zlqxrgzabv2uoc0oxyslqrd5sfxgsuvp Usqp Cau
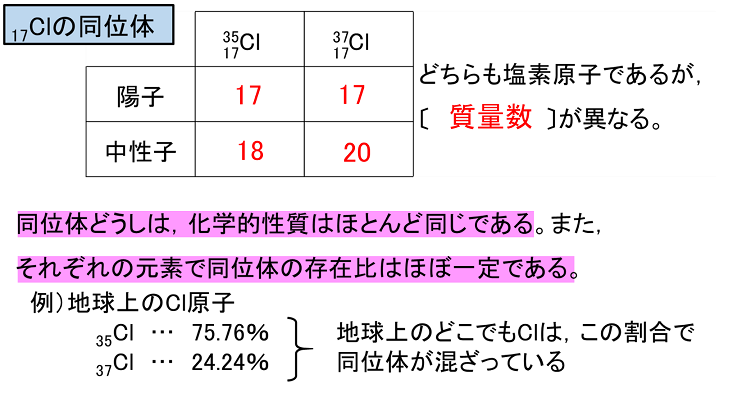



原子とその構造



Spring 8 で元素と地球をつなぐ エアロゾル中の鉄 Fe から 元素の循環 を覗く 分子地球化学 Spring 8 Web Site
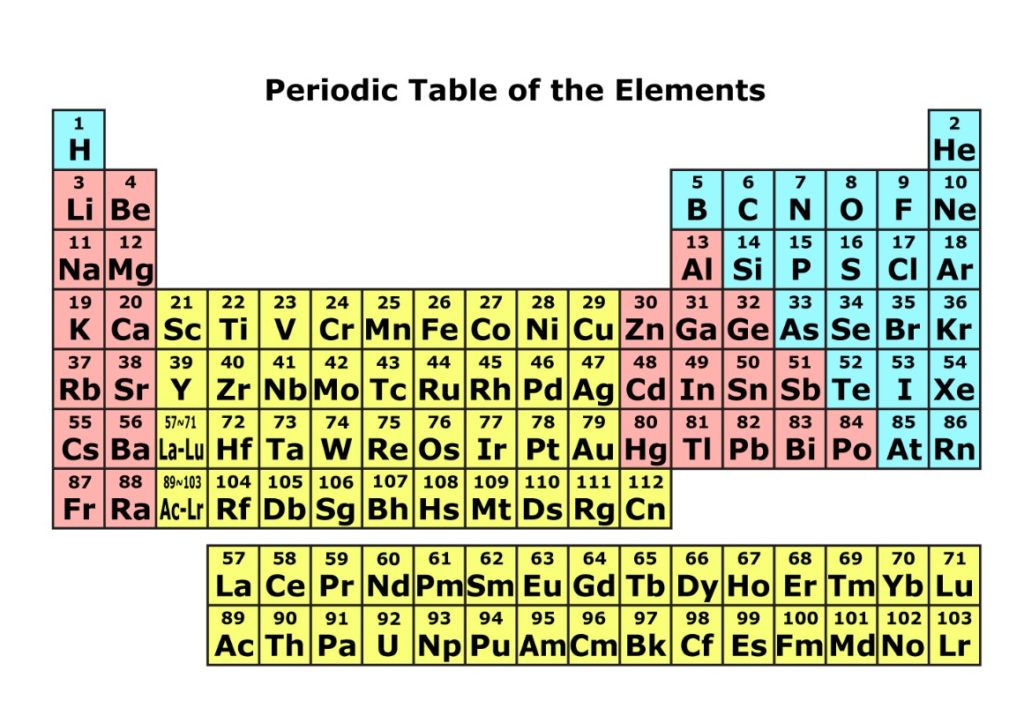



これで完璧 絶対に失敗しない周期表の覚え方




株式会社 マテリアルハウス 金属あれこれ 周期表




ジゃポニウム バンコクジジイのたわ言
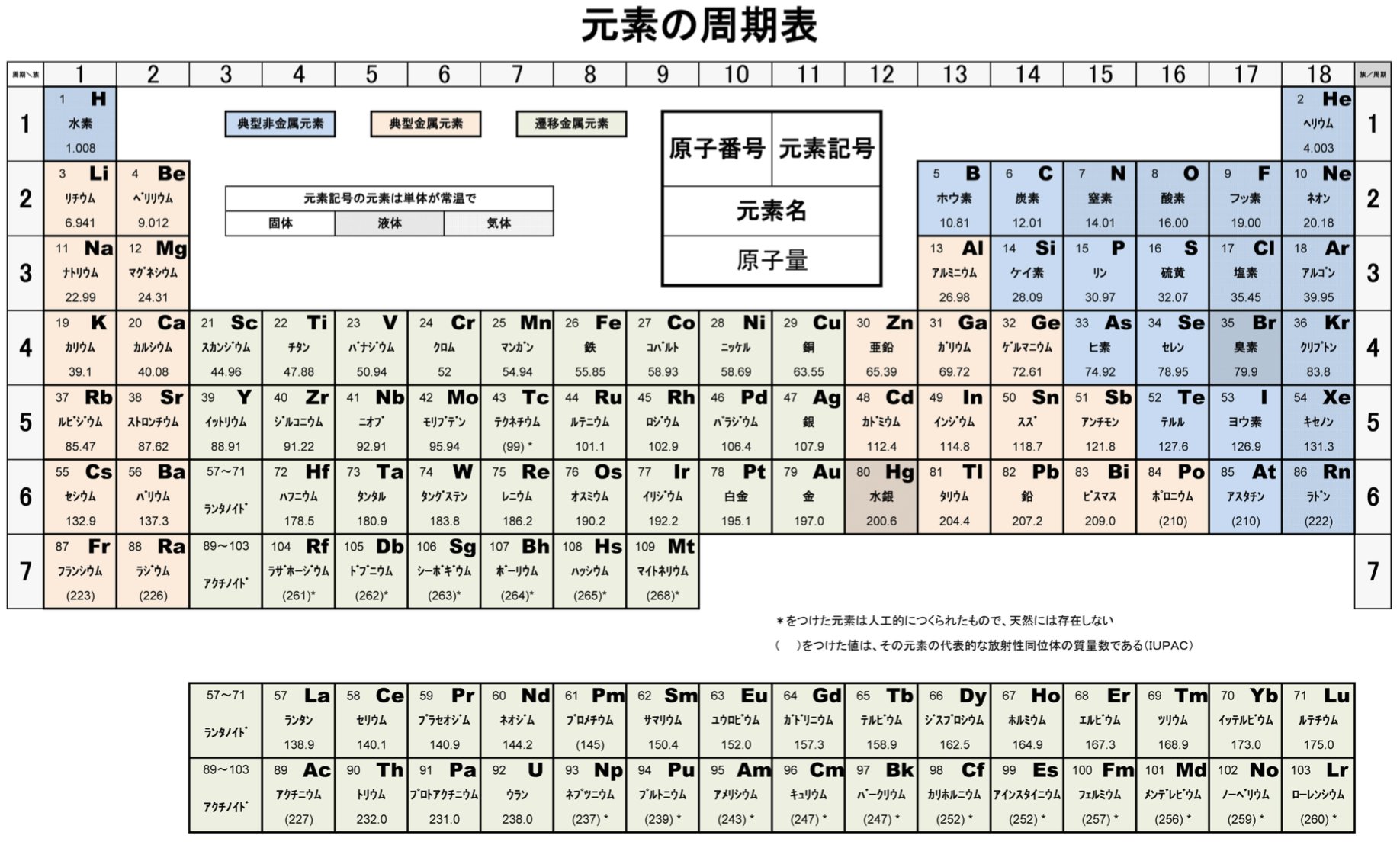



ひでと Quimica化学講師 Auf Twitter 自分なりに見やすい 周期表 作ってみたので良かったら使ってください ちなみにセンター試験は 原子番号まで 2次試験は原子番号36までと1族 2族 17族 18族全部が必須です Rtした人全員フォローする 勉強垢 化学



Numb016



元素の周期表
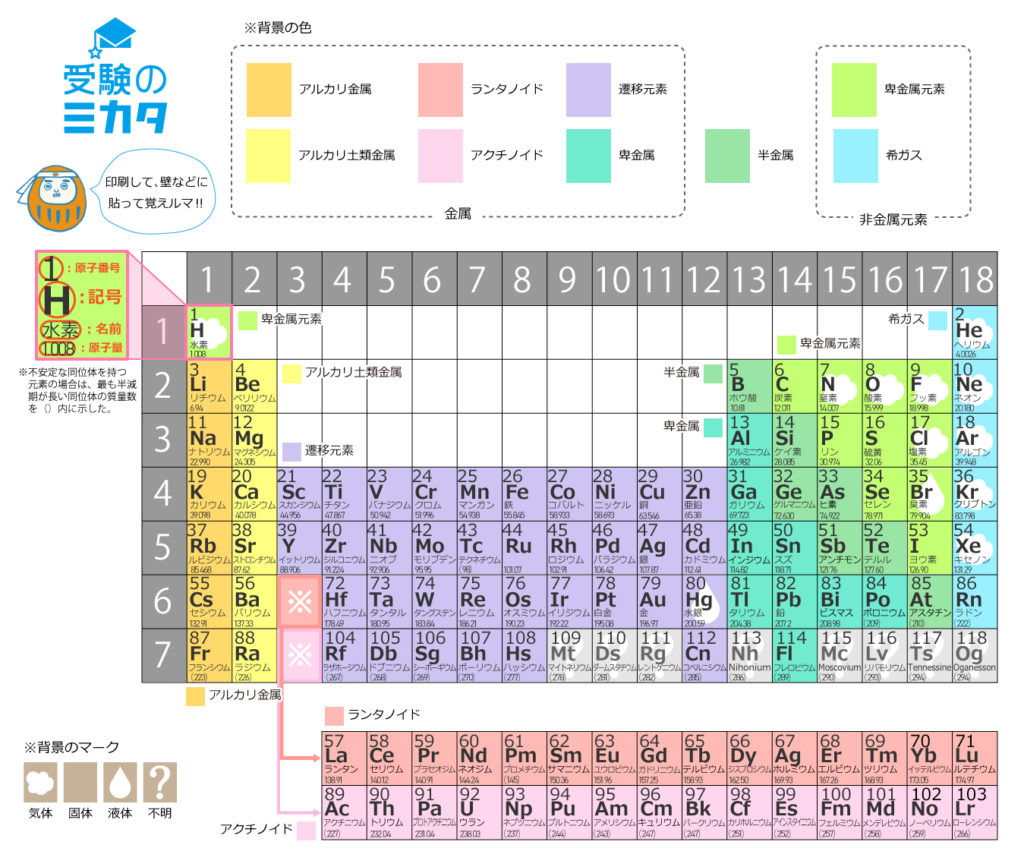



物質構造の基本 原子と分子 単体と化合物 ふかラボ
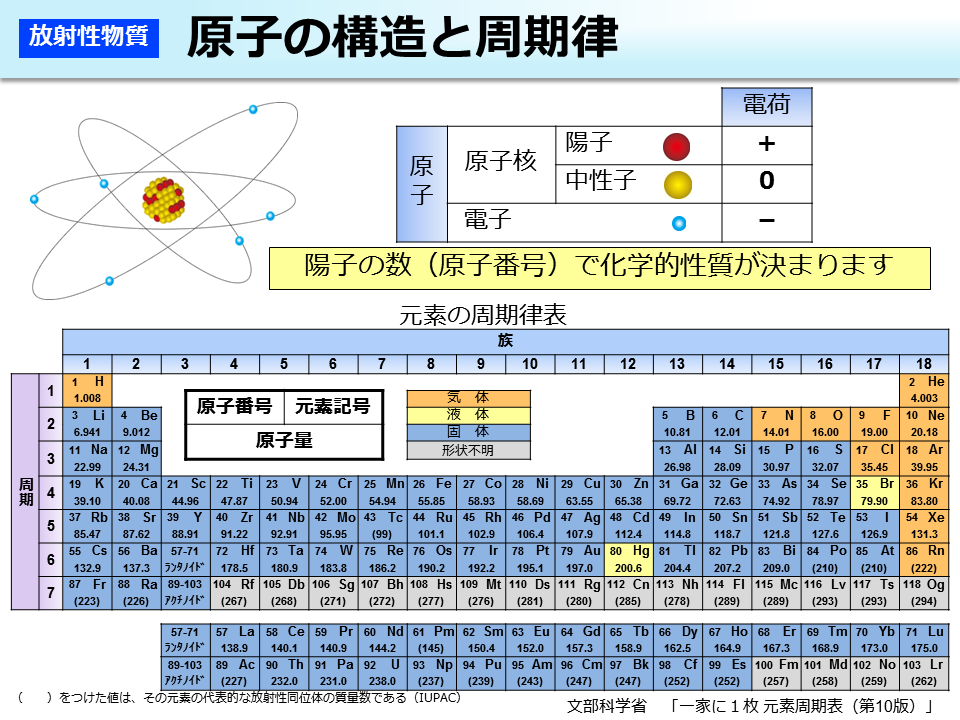



環境省 原子の構造と周期律



Www Env Go Jp Chemi Rhm H30kisoshiryo Attach 1903mat1 01 5 Pdf




周期表 Ptable



Www Osaka C Ed Jp Kanan Jishu E6 94 E7 Bf 92 E5 8c 96 E5 Ad A6 E5 9f Ba E7 8e E5 8f E8 80 97 E2 91 A1 Pdf



Ten Tokyo Shoseki Co Jp Spl Hl Support Files Kou E6 94 B9 E8 A8 E5 8c 96 E5 Ad A6 E5 9f Ba E7 8e 1 E7 A E7 Ab A0 E5 8e 9f E5 Ad 90 81 Ae E6 8b E9 80 A0 81 A8 E5 85 E7 B4 A0 81 Ae E5 91 A8 E6 9c 9f E8 A1 A8 Pdf



月の資料館 元素の周期表




周期表 会社員の化学物質管理ログ



原子とその構造 化学コラム




元素周期表 見やすい表で覚え方と元素を解説 ゴロ合わせも 高校生向け受験応援メディア 受験のミカタ
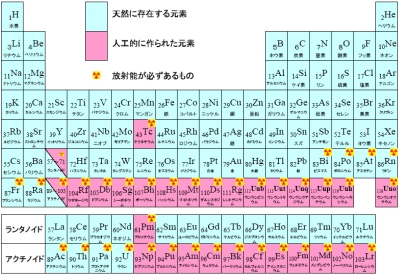



重元素の基礎知識 大阪大学 篠原研究室
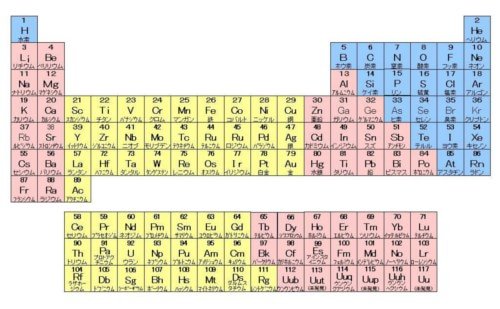



元素の周期律表とは 元素記号とは わかりやすく解説 科学をわかりやすく解説




これは 暗記するしかないですか 質量数なのど 暗記してないと書けないですよね Clear



宇宙 時間 空間 素粒子 周期表 電子軌道 他 14年現在の素粒子 宇宙の理解 ページ下部の 物質の性質を知ろう も見て下さい ものづくり 相手を知れば対応の仕方が解る リンク切れはお知らせください 物質の性質を知ろう 先ずは 周期表 そして
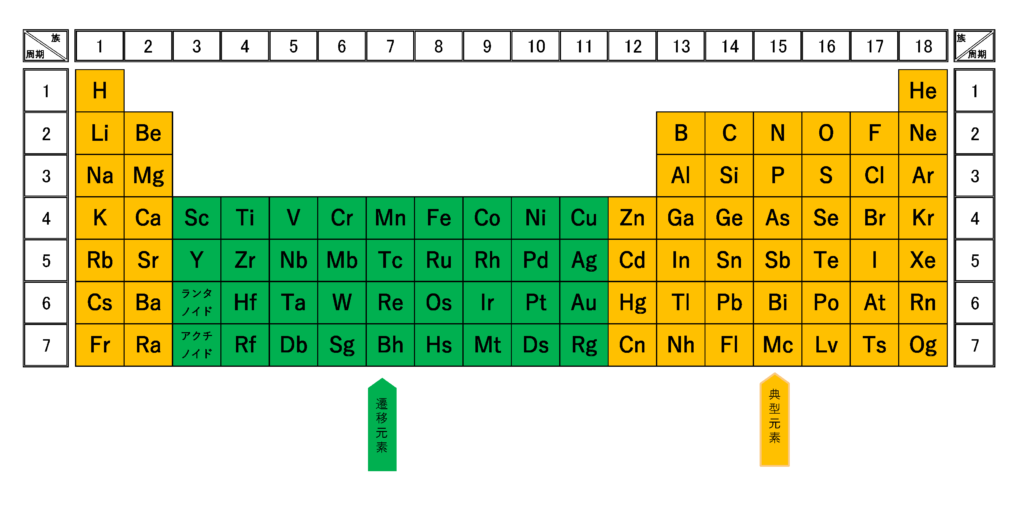



完全版 周期表の語呂合わせの覚え方と族 縦 や周期 横 の見方 サイエンスストック 高校化学をアニメーションで理解する



Ten Tokyo Shoseki Co Jp Spl Hl Support Files Kou E6 94 B9 E8 A8 E5 8c 96 E5 Ad A6 E5 9f Ba E7 8e 1 E7 A E7 Ab A0 E5 8e 9f E5 Ad 90 81 Ae E6 8b E9 80 A0 81 A8 E5 85 E7 B4 A0 81 Ae E5 91 A8 E6 9c 9f E8 A1 A8 Pdf
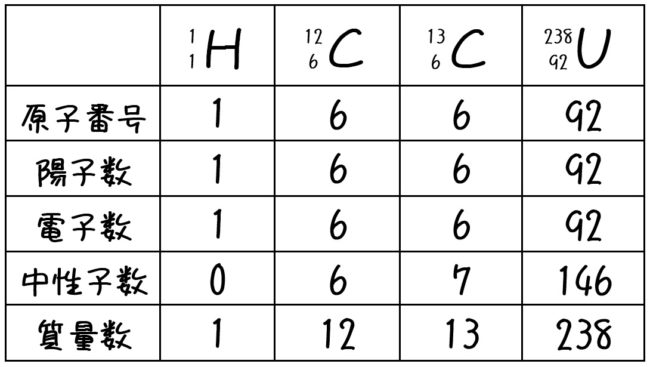



化学基礎 原子の構造 原子番号 質量数 Tekibo
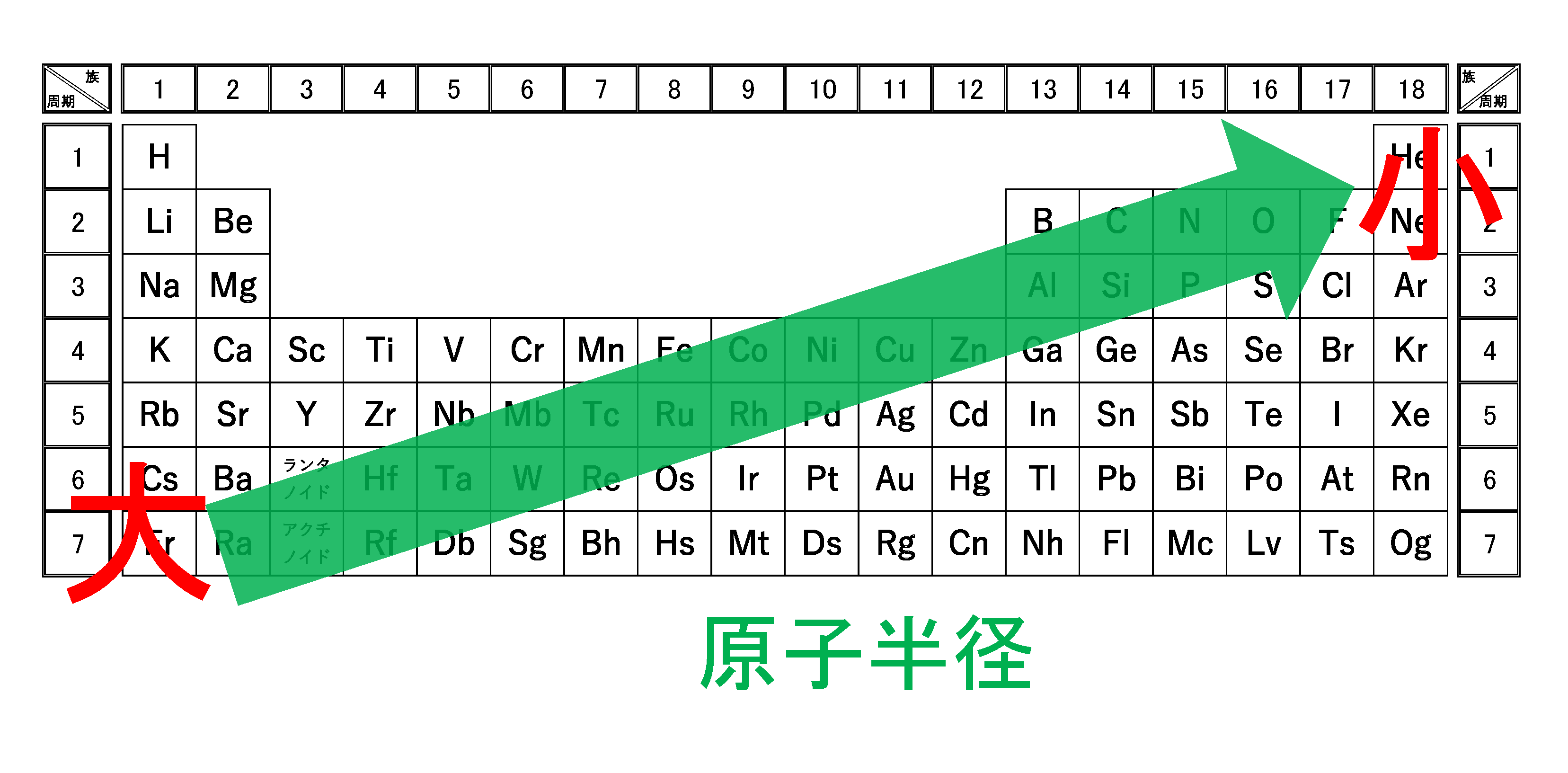



3分でわかる 原子半径 原子の大きさ の周期表での大小関係とその理由を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する



何故元素表の水素 ベリリウム マグネシウムの後は空欄が続くのですか Quora
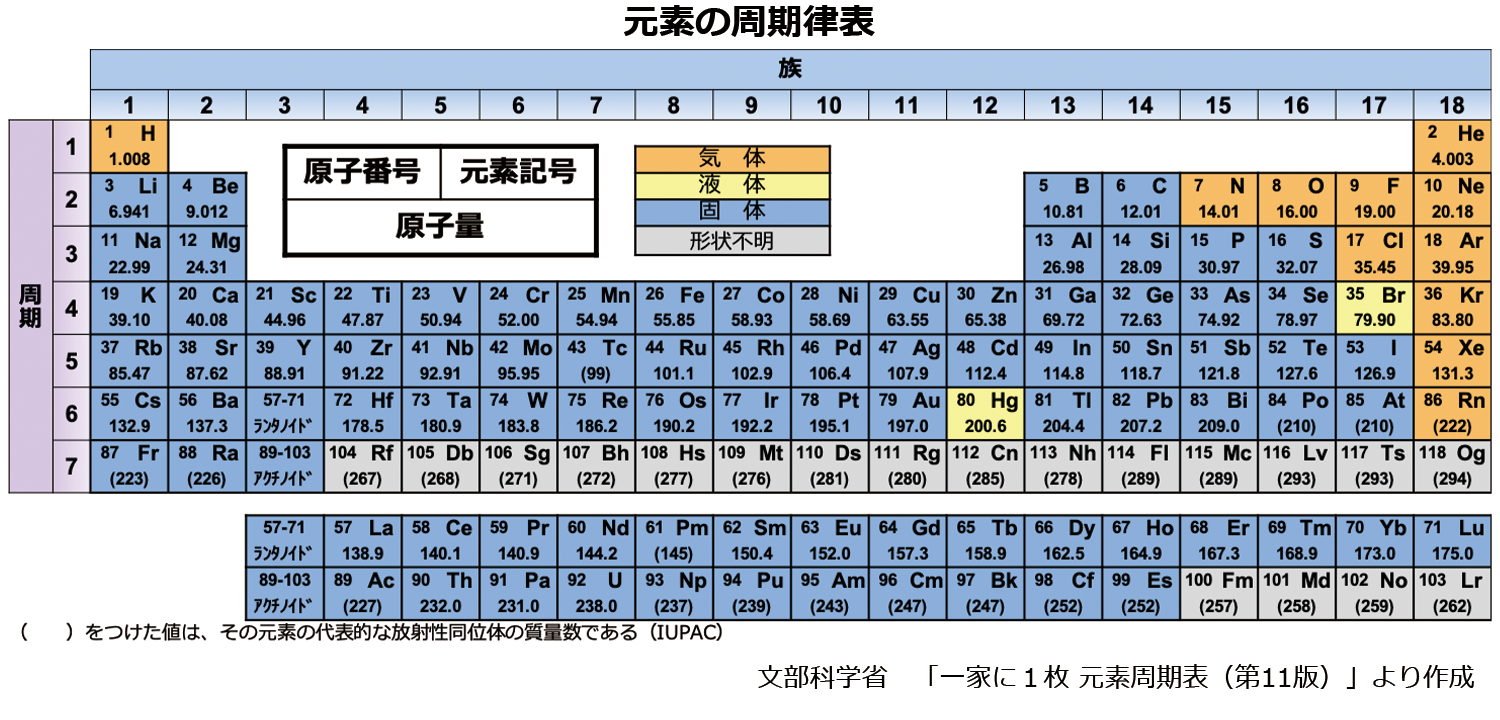



環境省 原子の構造と周期律




元素周期表 元素周期律表 自然元素と人工元素 Arealink



基礎化学




高校化学基礎 原子番号と質量数 映像授業のtry It トライイット




同素体と同位体の違い 意味 種類など間違えやすい所を覚えやすく


コメント
コメントを投稿